Dobivanje i primjena koloidnih sustava
Dobivanje koloidnih sustava
Priprema koloidnih čestica može se postići na nekoliko načina.
Jedan način je
Prema veličini čestica, koloidne sustave dijelimo na
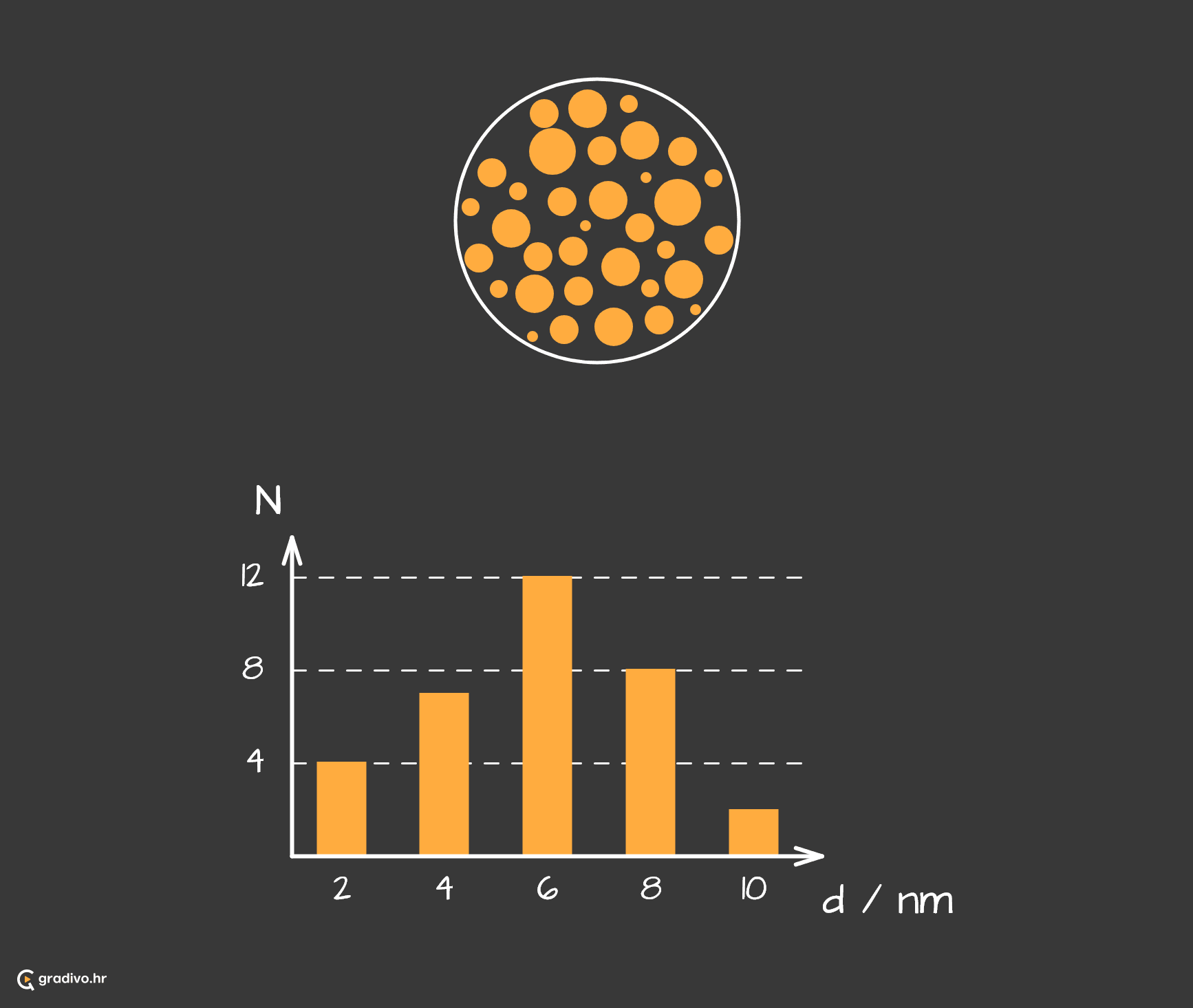
Drugi način je
Ag+(aq) + Cl−(aq) → AgCl(s)
Tako nastaju male čestice AgCl koje čine koloid.
Naboj na površini koloidne čestice može biti
Pozitivan površinski naboj nastaje kada čestica privuče više kationa nego aniona. Na primjer, dodatkom Ag+ iona, čestica postaje pozitivno nabijena.
Negativan površinski naboj nastaje kada čestica privuče više aniona nego kationa. Primjer toga je dodatak Cl− iona, gdje površina čestice postaje negativno nabijena.

Ovi naboji na površini koloidnih čestica igraju
Primjena koloidnih sustava
Adsorpcija
A(aq) ⇌ A(ads).

U ovom kontekstu,
Adsorpcija iona na površinu može promijeniti stanje u međupovršinskom sloju, kao i točku nul-naboja, odnosno izoelektričnu točku.
Adsorpcijom aniona, površina postaje negativnija, a izoelektrična točka se pomiče prema nižim pH-vrijednostima.
Adsorpcijom kationa, površina postaje pozitivnija, a izoelektrična točka pomiče se prema višim pH-vrijednostima.
Ove promjene mogu značajno utjecati na svojstva koloidnog sustava i njegovu stabilnost.
Adsorpcija se koristi u različitim industrijama i procesima zbog svoje sposobnosti vezanja molekula na površine čvrstih tvari. Ovaj proces igra ključnu ulogu u pročišćavanju zraka ili plinova (npr. u plinskim maskama ili različitim filtrima, gdje se štetne molekule adsorbiraju na površinu čvrstih tvari) te katalizi (adsorpcija smanjuje energiju aktivacije određenih kemijskih reakcija, čime se povećava brzina reakcije).
Osim toga, adsorpcijom molekula mijenjaju se svojstva površina, što je korisno u raznim primjenama. U farmaciji – kod razvoja lijekova koji djeluju adsorpcijom aktivnih tvari,
u medicini – kod stvaranja biokompatibilnih implantata koji adsorbiraju molekule za bolju interakciju s tkivom, u tekstilnoj industriji – za vezanje boja na tkanine ili proizvodnju nemočivih materijala kroz adsorpciju određenih kemijskih spojeva.
Površinski aktivne tvari
Kada se površinski aktivne tvari dodaju u vodu, njihove molekule se orijentiraju na međupovršini. Na primjer, kada se surfaktant doda u smjesu ulja i vode, polarni dio molekule surfaktanta okrenut će se prema vodi, dok će nepolarni repovi biti usmjereni prema ulju. Ova orijentacija molekula stvara stabilan sloj koji smanjuje međumolekulske sile na površini.

Kada se dodaju površinski aktivne tvari, kao što su sapuni ili deterdženti, molekuli se nakupljaju na nekoliko važnih međupovršina, uključujući međupovršinu vode i zraka te međupovršinu vode i stijenke čaše.
Ove promjene značajno utječu na površinska svojstva vode. Na primjer, dodavanje surfaktanta smanjuje površinsku napetost vode, što rezultira time da tekućina na podlozi poprima oblik kapljice. Oblik kapljice ovisi o napetosti međupovršina, bilo da se radi o: tekućini/plinu, tekućini/čvrstoj podlozi ili čvrstoj podlozi/plinu.
Dodatkom površinski aktivne tvari, kapljica se na površini širi, što dodatno poboljšava njeno prodiranje i raspršivanje u drugim tekućinama ili na čvrstim površinama. Ovaj fenomen ima brojne primjene, uključujući čišćenje, emulgiranje i stabilizaciju sustava u kemijskoj i prehrambenoj industriji.
Kritična micelizacijska koncentracija (CMC) predstavlja važnu točku u ovom procesu. To je koncentracija površinski aktivne tvari iznad koje počinju nastajati micele. Kada koncentracija surfaktanta u otopini pređe CMC, molekuli počinju formirati micele, čime se povećava njihova sposobnost za uklanjanje nečistoća.
Micele imaju ključnu ulogu u uklanjanju nečistoća iz otopine. U njima se otapaju različite vrste nečistoća, uključujući kapljice ulja te različite nečistoće prisutne u vodi.
Ova sposobnost micele da vezuju i uklanjaju nečistoće čini ih izuzetno korisnim u raznim aplikacijama, osobito u kućanstvu i industriji.
Emulzije i emulgatori
Ove molekuli smanjuju površinsku napetost na granici dviju faza, čime se olakšava stabilizacija emulzija. Smanjenje površinske napetosti omogućuje disperziju jedne tekućine unutar druge, stvarajući stabilnu emulziju koja se ne razdvaja.
Emulgatori imaju široku primjenu u različitim industrijama, uključujući:
- proizvodnju lijekova: Gdje pomažu u stvaranju stabilnih farmaceutskih preparata.
- prehrambena industrija: U proizvodima poput majoneze i emulzija, gdje je stabilnost ključna.
- kozmetički proizvodi: Gdje emulgatori omogućuju postizanje željenih svojstava i stabilnosti krema i losiona.
U nestabilnoj emulziji, tekućine se brzo razdvajaju, uzrokujući taloženje dispergirane faze.
U stabilnoj emulziji, emulgatori osiguravaju da se dispergirane kapljice ravnomjerno raspoređuju unutar kontinuirane faze, sprječavajući njihovo razdvajanje i taloženje.
Ovaj proces omogućava stvaranje i očuvanje emulzija u raznim proizvodima koji su sastavni dio svakodnevnog života.
Odvajanje čestica koloidnih sustava
Ultrafiltracija
Elektroforeza
Dijaliza
Posebna vrsta dijalize jest
Sedimentacija
Isprobaj potpuno besplatno!
Registracijom dobivaš besplatan*
pristup dijelu lekcija za svaki predmet.




