Kemija - 2022. jesen, 7.
Crtežom je prikazan pokus otapanja soli u vodi gdje je X simbol nekoga halogenog elementa.
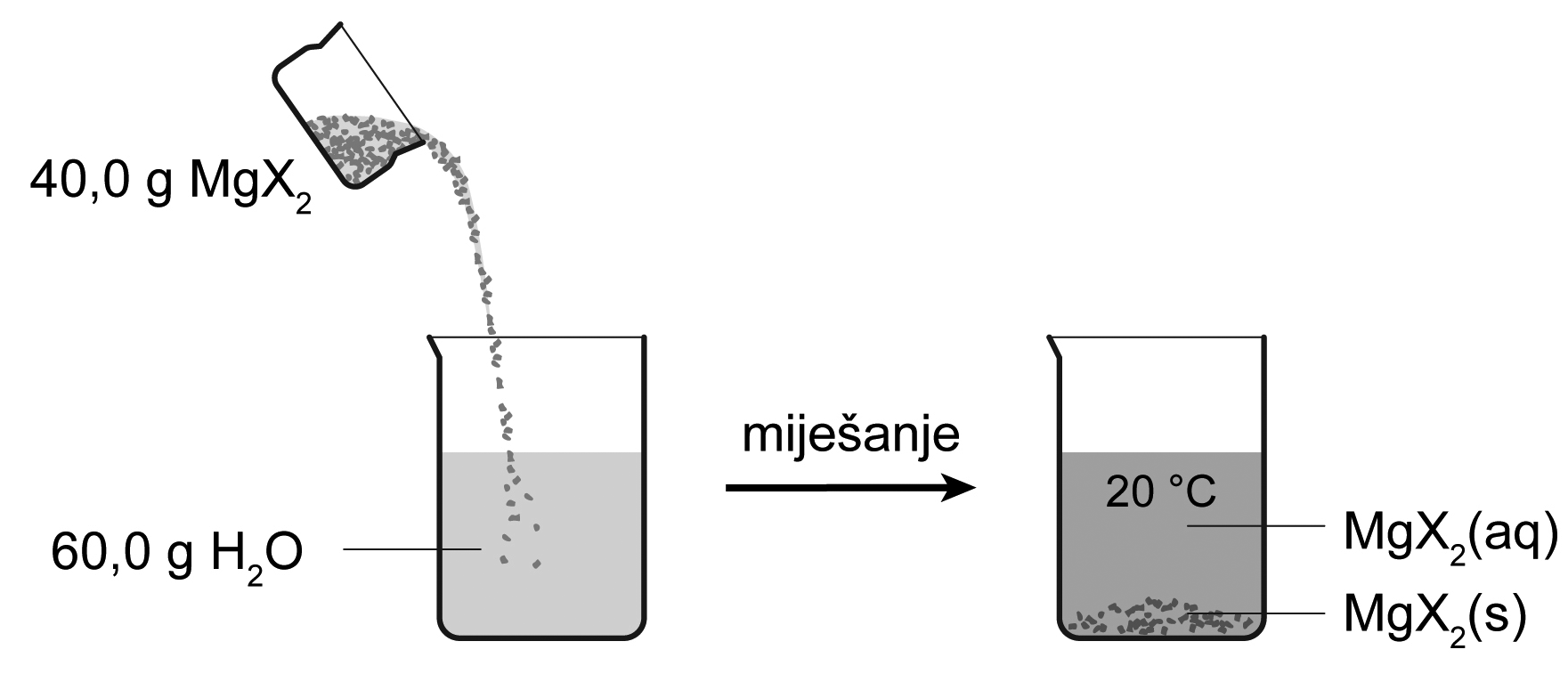
U 100 g vode pri 20 °C može se otopiti najviše 54,6 g te soli.
Izračunajte masu otopljene magnezijeve soli u čaši nakon uspostavljanja ravnotežnoga stanja pri 20 °C.
Izračunajte maseni udio otopljene magnezijeve soli u otopini nakon uspostavljanja ravnotežnoga stanja pri 20 °C.
Dodatkom vodene otopine srebrova nitrata u vodenu otopinu magnezijeve soli nastaje bijeli sirasti talog. Napišite kemijski naziv magnezijeve soli .